Ideas Para Trabajos Investigativos
Cómo Funcionan las Baterías
Una batería es escencialmente una lata llena de químicos que producen
electrones. Las reacciones químicas son capaces de producir electrones
que son llamados reacciones electroquímicas.
Si se examina una batería, esta tiene dos terminales. Una terminal está marcada (+) positivo mientras la otra está marcada (-) negativo. En una AA, o C (baterías más comunes) los extremos son los terminales. En una batería de auto existen dos grandes tubos que actúan de terminales.
Los electrones se agrupan en la terminal negativa de la batería. Si se conecta un cable entre las terminales positivas y negativas, los electrones pasarán de la terminal negativa a la positiva tan rápido como puedan (y descargarán a la batería muy rápido -esto también tiende a ser peligroso, especialmente con baterías grandes, así que no es algo que debería hacer-). Normalmente se coloca algún tipo de artefacto a la batería con el cable. Este artefacto puede ser una bombilla, un Motor, un circuito electrónico como un radio, etc.
Dentro de la batería misma, una reacción química produce electrones, y la velocidad de la producción de electrones hecha por esta reacción (la resistencia interna de la batería) controla cuántos electrones pueden pasar por las terminales. Los electrones pasan de la batería al cable, y deben viajar de la terminal negativa a la positiva paa que la reacción química se lleve a cabo. Es por eso que que una batería puede guardarse por un año y todavía conserva su energía plenamente -a menos que los electrones corran hacia la terminal positiva, la reacción química no se efctuará-. Una vez que se conecte el cable, la reacción empieza.
Química de Baterías
Si desea aprender acerca de las reacciones electroquímicas que utilizan
las baterías, será fácil ejecutar experimentos en casa para probar
diferentes combinaciones. Para hacer esos experimentos con precisión,
debería comprar un medidor de voltios-ohmnios en una tienda cercana. Asegúrese
de que el medidor pueda leer voltajes bajos (en el rango de 1 volt) y
corrientes bajas (en el rango de 5 a 10 miliamp). Así verá exactamente
qué es lo que hace su batería.
La primera batería fue creada por Alessandro Volta en 1800. Para crear su batería utilizó una pila alternando capas de cinc y plata, empleando papel secante empapado en agua salada como aislador. Así más o menos:
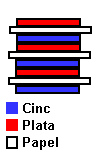
Este artefacto fue conocido como "pila voltaica". Las capas superior e inferior de la pila deben de ser de diferentes metales, como se muestra. Si ata un cable de arriba a abajo de la pila puede calcular un voltaje y una corriente. La pila puede seguir agrandándose tanto como quiera, y cada capa incrementará el voltaje por una cantidad determinada. Puede crear su propia pila voltaica utilizando monedas y toallas de papel. Mezcle sal con agua (toda la sal posible que el agua pueda soportar) y empape el papel en esta mezcla. Entonces cree una plia alternando entre diferentes metales. Observe qué tipo de voltaje y corriente produce la pila. Trate con diferentes números de capas y observe qué efectos tiene en el voltaje. Entonces trate alternando entre monedas y vea qué pasa. Otras combinaciones incluyen al acero y al aluminio. Cada combinación metálica produce un voltaje levemente diferente.
Otro experimento simple que puede tratar es utilizar un frasco de compota para bebé, un ácido diluído, cables y clavos. Llene el frasco con jugo de limón o vinagre (diluya los ácidos) y coloque un clavo y un pedazo de cable de cobre en el frasco de manera que no lo toque (el cable entre un clavo y otro). Utilize clavos galvanizados y de hierro. Entonces calcule el voltaje y corriente atando su voltímetro a las 2 piezas de metal. Cambie el jugo de limón por agua salada, y utilice diferentes clavos y metales para ver el efecto.
Las baterías modernas utilizan una variedad de químicos para realizar sus reacciones. La química de las baterías comunes incluyen:
- Baterías de Cinc, también conocidas
como baterías estándar de carbón. La química de cinc-carbón es
utilizada en cualquier batería AA, o afín. Los electrodos son de
cinc y carbón, con una unión ácida entre ellas como electrolito.
- Baterías alcalinas. Los electrodos son
de cinc y óxido de manganeso con un electrolito alcalino.
- Batería de níquel-cadmio. Utiliza el
hidróxido de níquel y electrodos de cadmio con hidróxido de potasio
como electrolito. Es recargable.
- Hidruro de níquel-metal. Recargable.
Reemplazó rápido al níquel-cadmio porque no sufre de los problemas
que tiene la anterior.
- Ion-litio. Recargable. Muy buen
porcentaje de poder-peso, se utiliza en los últimos PC's portátiles
y teléfonos celulares.
- Plata-cinc. Utilizada en aplicaciones aeronáuticas porque el porcentaje de poder-peso es bueno.
Detalles de baterías
Actualmente, casi ningún dispositivo utiliza una celda por vez, una celda
es un conjunto de materiales que generan voltaje y corriente (como el cinc
y el carbón) que están agrupados y cubiertos por un material aislante.
Si abrimos una batería encontraremos las celdas dentro. Una celda es más
o menos así:
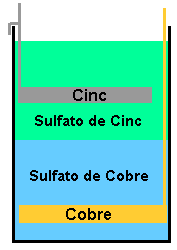
Normalmente las baterías se agrupan en serie para obtener altos voltajes o en paralelo para altas corrientes. El siguiente diagrama muestra esos arreglos:
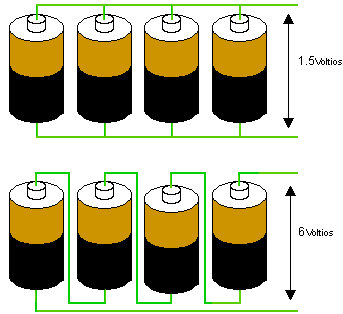
El arreglo de arriba es llamado en Paralelo.
Si asume que cada celda produce 1.5 voltios, entonces 4 baterías en
paralelo también producirán 1.5 voltios pero la corriente será
cuatro veces mayor. En arreglo de abajo es llamado
en Serie. Los cuatro voltajes se suman
para producir 6 voltios.

